في إنجاز علمي يُعد من أبرز اختراقات الطب الحديث، تُوّج العالمان سوي لاي ثين من المعهد الوطني الأمريكي للقلب والرئة والدم (NHLBI)، وستيوارت أوركين من جامعة هارفارد بجائزة "الاختراق في علوم الحياة" البالغة 3 ملايين دولار، تقديراً لأبحاثهما التي مهّدت الطريق لأول علاج جيني فعّال لاضطرابات الدم الوراثية باستخدام تقنية كريسبر لتحرير الجينات.
الجائزة جاءت تتويجاً لمسار علمي طويل قاد إلى تطوير علاج جيني يُعرف باسم "كاسغيفي"، والذي يمثل أول محاولة ناجحة لعلاج وظيفي لأمراض معقدة مثل فقر الدم المنجلي والثلاسيميا بيتا، بحسب "لايف ساينس".
هذا العلاج لا يكتفي بتخفيف الأعراض، بل يعالج جذور المرض عبر تعديل جيني دقيق، يعيد للجسم قدرته على إنتاج نوع من الهيموغلوبين كان نشطاً في مرحلة الطفولة المبكرة.

تسلّم ثين وأوركين جوائزهما في حفل أقيم في لوس أنجليس، السبت الماضي.
وتُمنح جائزة الإنجازات الرائدة في علوم الحياة منذ عام 2013 تقديراً للإنجازات في علوم الحياة .
فكرة غيرت مسار الطب
القصة بدأت بسؤال علمي بسيط: "لماذا يعاني بعض المرضى من أعراض أخف من غيرهم؟"، قاد هذا التساؤل الباحثة سوي لاي ثين إلى اكتشاف دور جين يُعرف باسم "BCL11A"، يعمل كمثبط لإنتاج "الهيموغلوبين الجنيني" مع التقدم في العمر.
وبالتعاون مع أبحاث ستيوارت أوركين، تم التوصل إلى أن تعطيل هذا الجين يمكن أن يعيد تشغيل إنتاج هذا النوع من الهيموغلوبين، ما يخفف بشكل جذري من تأثير الأمراض.
 مضاد اكتئاب شائع يتسبب في تآكل جلد امرأة بنسبة 55% - موقع 24في حادثة طبية صادمة، كادت امرأة تبلغ من العمر 42 عاماً أن تفقد حياتها بعد تعرضها لتفاعل دوائي شديد الخطورة عقب تناولها عقار "لاموتريجين"، المستخدم في علاج اضطرابات المزاج، ما أدى إلى تقشر وفقدان نحو 55% من جلدها.
مضاد اكتئاب شائع يتسبب في تآكل جلد امرأة بنسبة 55% - موقع 24في حادثة طبية صادمة، كادت امرأة تبلغ من العمر 42 عاماً أن تفقد حياتها بعد تعرضها لتفاعل دوائي شديد الخطورة عقب تناولها عقار "لاموتريجين"، المستخدم في علاج اضطرابات المزاج، ما أدى إلى تقشر وفقدان نحو 55% من جلدها.
كيف يعمل العلاج؟
يعتمد العلاج على خطوات معقدة لكنها فعّالة:
- سحب خلايا من نخاع عظم المريض.
- تعديلها جينيًا باستخدام تقنية كريسبر لتعطيل الجين المثبّط.
- إعادة حقن الخلايا المعدلة في الجسم.
لتبدأ بعدها بإنتاج خلايا دم صحية قادرة على حمل الأكسجين بكفاءة، دون التشوهات المميزة لهذه الأمراض.
رغم الأمل الكبير الذي يحمله هذا العلاج، إلا أن تطبيقه لا يزال محدوداً، حيث يستغرق نحو عام كامل، ويتطلب علاجاً كيميائياً قاسياً تصل تكلفته إلى ملايين الدولارات، ما يجعله بعيد المنال عن ملايين المرضى، خصوصاً في أفريقيا وآسيا، حيث تنتشر هذه الأمراض بشكل واسع.
نحو مستقبل أكثر بساطة
يدفع هذا الواقع العلماء للبحث عن بدائل أكثر سهولة، مثل تقنيات التعديل الجيني داخل الجسم مباشرة، دون الحاجة إلى إجراءات معقدة، كما يجري تطوير أدوية أقل تكلفة وأكثر قابلية للتوزيع، لتوسيع نطاق الاستفادة.

ورغم التحديات، يمثل هذا الإنجاز نقطة تحول في تاريخ علاج الأمراض الوراثية، إذ يفتح الباب أمام عصر جديد من الطب القائم على تعديل الجينات.
مرض فقر الدم المنجلي
يُشار إلى أن "مرض فقر الدم المنجلي"، يُصيب ما بين 7 إلى 8 ملايين شخص حول العالم، غالبيتهم في أفريقيا، لدى المصابين بهذا المرض، تتخذ خلايا الدم الحمراء شكلاً هلالياً مميزاً، وذلك لأن الهيموغلوبين، وهو الجزيء الحامل للأكسجين داخل الخلايا، يُشكّل أليافاً طويلة وصلبة تُشوّه شكل الخلايا.
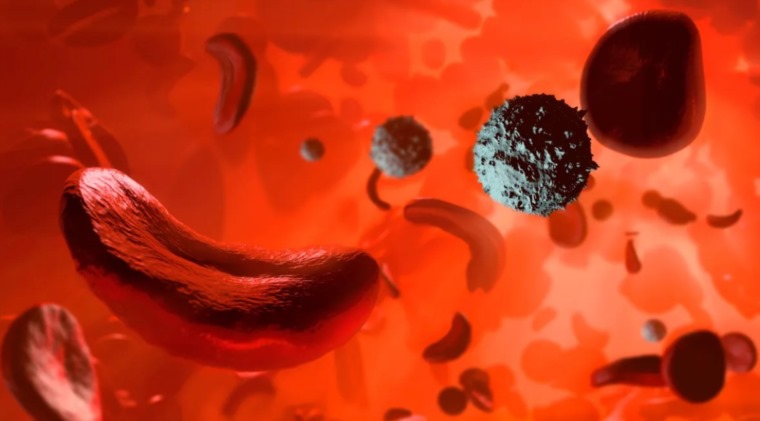
تلتصق هذه الخلايا المنجلية ببعضها، مما يُؤدي إلى تكوّن جلطات دموية، كما أنها تنفجر وتموت بسهولة، مما يُسبب انخفاضاً في عدد خلايا الدم الحمراء، وغالباً ما يواجه المرضى نوبات ألم حادة، تُعرف باسم "الأزمات"، عندما تسد خلايا الدم الحمراء الأوعية الدموية.
يمكن أن تُلحق هذه الانسدادات الضرر بأعضاء مثل الرئتين والكبد والطحال، كما يمكن أن تؤدي الانسدادات في الرئتين إلى "متلازمة الصدر الحادة"، التي تُسبب انخفاضاً حاداً في مستويات الأكسجين، وهي السبب الرئيسي للوفاة لدى مرضى فقر الدم المنجلي .